A terapia com células CAR-T é um tratamento inovador que utiliza as células de defesa do próprio paciente, chamadas linfócitos T, para combater o câncer. Essas células são retiradas do paciente, modificadas em laboratório e, em seguida, retornam ao corpo para atuar diretamente no combate à doença.
Desenvolvida inicialmente nos Estados Unidos, a terapia CAR-T começou a ser testada em pacientes com câncer terminal no início dos anos 2010. Os resultados promissores levaram a Food and Drug Administration (FDA), agência reguladora dos Estados Unidos, a aprovar o uso da terapia CAR-T em 2017. No ano seguinte, em 2018, os cientistas responsáveis pela descoberta, James P. Allison e Tasuku Honjo, receberam o Prêmio Nobel de Medicina por suas contribuições à área.
No Brasil, a terapia CAR-T é estudada e aplicada por instituições como o Centro de Terapia Celular da USP, o Instituto Nacional de Câncer (INCA) e o Hospital Albert Einstein, AC Camargo Cancer Center, entre outras. Além disso, já existem produtos CAR-T aprovados pela ANVISA para comercialização no Brasil. A primeira aprovação ocorreu em 2022, e, desde então, quatro produtos já foram aprovados para comercialização no mercado brasileiro.
Segundo a ANVISA, os produtos de terapia avançada (como CAR-T) são medicamentos biológicos, obtidos a partir de células humanas, e devem seguir normas rigorosas de qualidade e segurança. Um dos diferenciais desse tratamento é que ele é feito a partir das células do próprio paciente, com a coleta sendo realizada no hospital que vai realizar o tratamento.
Esse processo exige uma colaboração intensa entre a indústria farmacêutica e os hospitais. Antes, a relação entre essas partes estava mais foca em pesquisas, educação e protocolos clínicos. Agora, com a terapia CAR-T, os hospitais se tornam fornecedores das células (denominadas “material de partida” pela ANVISA), que serão usadas pela indústria para fabricar o medicamento.
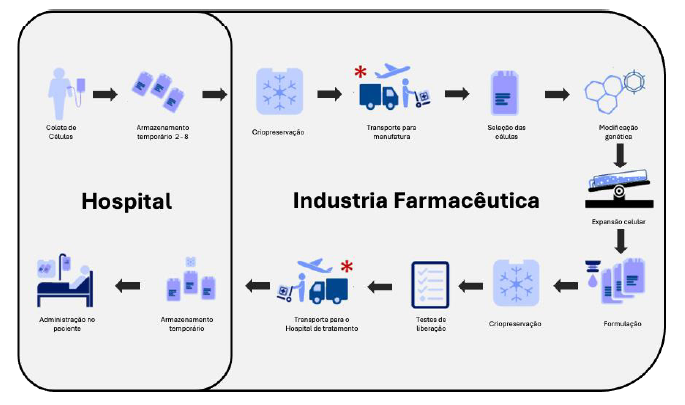
Para garantir que todos os aspectos do processo atendam aos mais altos padrões de qualidade e segurança, a cadeia de fabricação dos produtos CAR-T deve seguir os conceitos das boas práticas (GxP) aplicáveis a medicamentos, praticas estas já consolidadas para fabricação de outros tipos de medicamos como, biológicos, vacinas e genéricos. Esses princípios garantem que a fabricação e o uso das terapias sejam seguros e eficazes, desde a coleta das células até a entrega final do medicamento.
A ANVISA define requisitos específicos para a fabricação e coleta das células para produtos de terapia avançada nas seguintes normativas:
- IN 270/2023 – Estabelece as Boas Práticas de Fabricação para Produtos de Terapias Avançadas.
- RDC 836/2023 – Regula as Boas Práticas em Células Humanas para uso terapêutico e pesquisa clínica.
A ANVISA ainda clarifica no seu site que, a coleta do material celular que será material de partida para a fabricação de um produto de terapia celular avançada deve seguir o disposto na RDC 836/2023.
Esse cenário representa uma novidade no Brasil, pois os hospitais que coletam as células para fabricação de produtos de terapias celulares avançadas passam a ter de adotar os princípios GxP, conforme estabelecido pela ANVISA. Além das exigências regulatórias, as indústrias farmacêuticas frequentemente têm programas de qualificação e certificação para seus parceiros, o que implica que os hospitais também precisam atender a requisitos específicos de cada fabricante para garantir a qualidade do produto final.
Para assegurar que o hospital esteja em conformidade com as normas da ANVISA e os padrões exigidos pelos fabricantes de medicamentos CAR-T, é essencial que processos como:
- Garantia da Qualidade
- Treinamentos
- Registros e Integridade de Dados
- Validação de Processos e Sistemas
- Qualificação de Equipamentos
- Calibração
- Qualificação de Fornecedores
- Controle de Mudanças
- Não Conformidades e Ações Corretivas (CAPAs).
Estejam implementados e alinhados às normas e padrões aplicáveis.
Para que o Sistema de Qualidade (SGQ) do hospital esteja adequado às normas e padrões exigidos, contar com o suporte de profissionais experientes na área farmacêutica é um grande diferencial. Esse apoio pode ser crucial para agilizar o início da operação com a terapia CAR-T e evitar falhas que comprometam a qualidade e segurança do tratamento.
Se o hospital não possui profissionais com experiência na indústria farmacêutica, uma boa opção é buscar suporte diretamente com os fabricantes ou contratar consultores especializados, que são comuns no Brasil e oferecem serviços de alta qualidade para ajudar a cumprir as exigências regulatórias.
Conformidade Hospitalar com as Boas Práticas de Fabricação: Papel da Doctor Quality
A crescente adoção de terapias celulares avançadas, como a CAR-T, impõe aos hospitais desafios regulatórios rigorosos. Nesse contexto, a atuação da consultoria Doctor Quality tem sido essencial para garantir que instituições hospitalares estejam em conformidade com as Boas Práticas de Fabricação (BPF), especialmente nas atividades de coleta e processamento celular.
- Estruturação e Implantação do Sistema de Gestão da Qualidade (SGQ)
A Doctor Quality auxilia na criação ou aprimoramento do SGQ dos hospitais, assegurando o alinhamento com a RDC 658/2022, IN 270/2023 e RDC 836/2023. Isso inclui a implementação de procedimentos operacionais padrão (POPs), sistemas de gestão documental, rastreabilidade e integridade de dados. - Capacitação e Treinamento Contínuo
A consultoria oferece treinamentos técnicos voltados para a equipe hospitalar, com foco em GxP, biossegurança, integridade de dados e exigências regulatórias da ANVISA e dos fabricantes de CART. - Validação de Processos e Qualificação de Equipamentos
A Doctor Quality apoia na validação de processos críticos de coleta, transporte e armazenamento de células, bem como na qualificação de equipamentos como freezers, centrífugas e incubadoras, assegurando conformidade e reprodutibilidade. - Gestão de Riscos e Controle de Mudanças
A consultoria implementa abordagens baseadas em risco, conforme preconizado pela RDC 658, com uso de matrizes de risco, definição de planos de contingência e gestão estruturada de mudanças com impacto regulado. - Apoio na Implementação de Ações Corretivas e Preventivas (CAPAs)
Estrutura sistemas de investigação de desvios e não conformidades, com análise de causa raiz e planejamento eficaz de CAPAs para prevenção de recorrências. - Preparação para Auditorias e Inspeções
A Doctor Quality realiza simulações de inspeção, orienta em autoinspeções internas e prepara os hospitais para auditorias de qualificação por farmacêuticas e inspeções regulatórias da ANVISA. - Adequação a Requisitos Específicos de Fabricantes
Atua como elo técnico entre hospitais e fabricantes de CAR-T, promovendo ajustes nos processos hospitalares conforme exigências contratuais específicas.
Conclusão
A atuação da Doctor Quality é estratégica e essencial para assegurar que os hospitais estejam tecnicamente preparados e em plena conformidade regulatória para manipular produtos de terapias avançadas. Essa colaboração garante não apenas a segurança do paciente e a qualidade do produto, mas também a sustentabilidade das instituições no cenário regulatório atual.
Fonte(s):
https://www.gov.br/anvisa/pt-br/assuntos/sangue/terapias-avancadas
https://www.gov.br/anvisa/pt-br/acessoainformacao/perguntasfrequentes/sangue/ensaios-clinicos
https://butantan.gov.br/terapia-celular
https://www.gov.br/saude/pt-br/assuntos/noticias/2024/marco/saude-investe-mais-de-r-200-milhoes-em-pesquisas-com-terapia-para-tratamento-do-cancer





